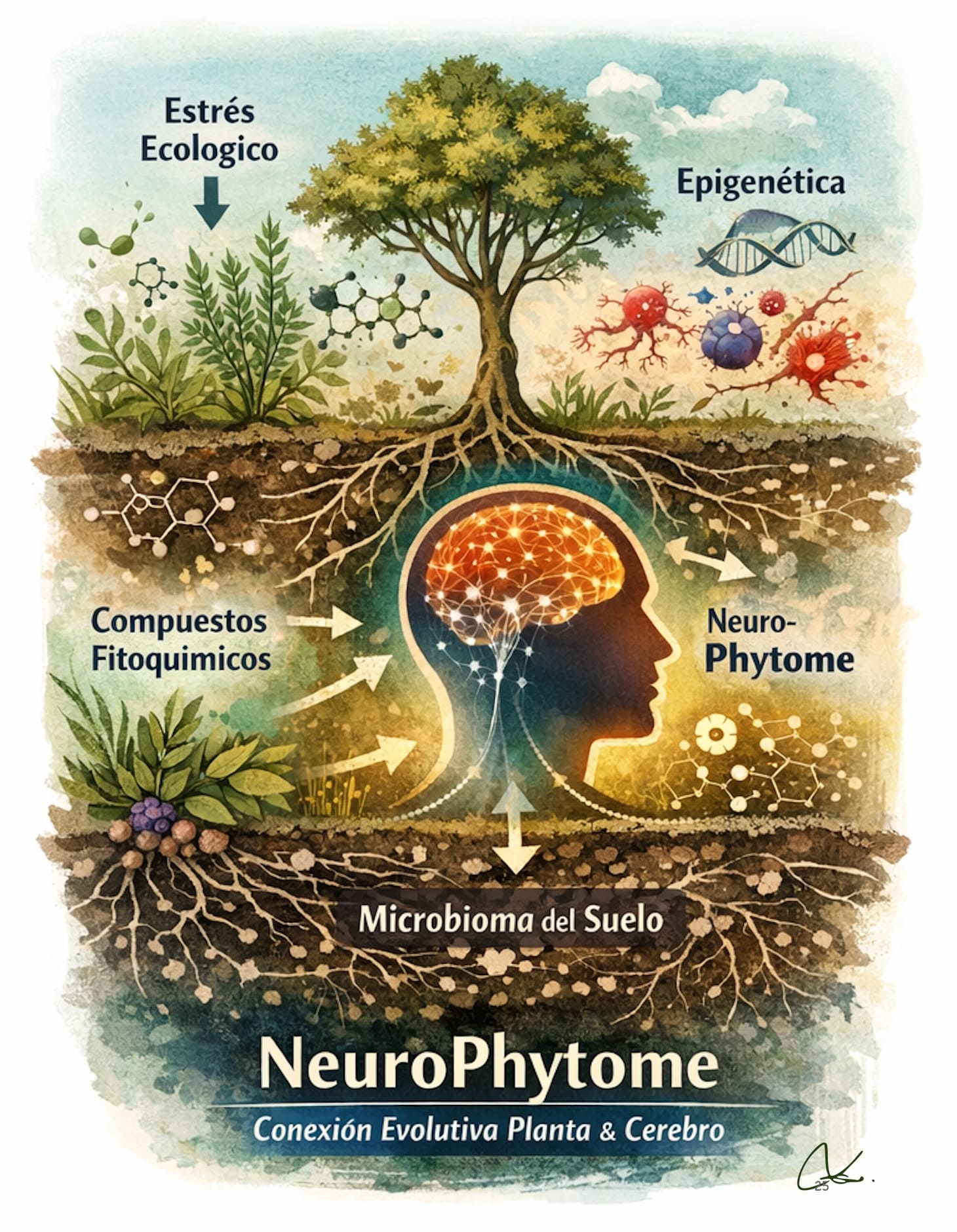
Cuando la medicina explica bien lo agudo, pero mal lo crónico
En la práctica clínica moderna hay una observación recurrente, rara vez formulada de manera explícita: una parte significativa de los problemas neurológicos, cognitivos y relacionados con el estrés no se explican bien mediante mecanismos agudos ni mediante déficits clásicos. Pacientes con diagnósticos similares, perfiles analíticos comparables y tratamientos correctamente indicados pueden mostrar trayectorias muy distintas. Algunos envejecen cognitivamente de forma relativamente estable; otros desarrollan deterioro progresivo. Algunos toleran décadas de estrés ambiental con escaso impacto funcional; otros muestran una fragilidad temprana difícil de objetivar.
La medicina contemporánea reconoce este problema. Conceptos como inflamación crónica de bajo grado, carga alostática, pérdida de reserva cognitiva o envejecimiento acelerado forman ya parte del lenguaje científico habitual (Franceschi et al., 2018; McEwen & Akil, 2020; Wyss-Coray, 2016). Sin embargo, los mecanismos que sostienen estos procesos siguen estando solo parcialmente integrados en la práctica clínica.
La farmacología moderna ha demostrado una enorme eficacia cuando existe un objetivo claro, un mecanismo dominante y una intervención definida. Pero muchos de los procesos que determinan la salud mental a largo plazo no se comportan de ese modo. No dependen de un fallo puntual, sino de desajustes regulatorios acumulativos, modulados por el entorno y el estilo de vida durante décadas.
Es en esta zona gris, entre la biología molecular y la experiencia clínica cotidiana, donde emerge la pregunta que da origen a NeuroPhytome.
Contenido
ToggleUna hipótesis de partida: la alimentación como modulador evolutivo de la fisiología humana
NeuroPhytome parte de una hipótesis simple en su formulación, pero exigente en sus implicaciones:
La alimentación, y en particular la alimentación de origen vegetal, no actúa únicamente como aporte de nutrientes o como factor de riesgo, sino como un proceso regulador de largo plazo que ha contribuido históricamente a moldear la fisiología humana, incluido el sistema nervioso.
Esta hipótesis no propone causalidades directas ni efectos terapéuticos inmediatos. Propone un cambio de escala temporal y conceptual. Sugiere que ciertos procesos fisiológicos solo pueden entenderse correctamente cuando se consideran exposiciones crónicas, acumulativas y contextuales, tal como ocurrió durante la mayor parte de la historia evolutiva humana.
Desde este punto de vista, la alimentación no es solo un acto repetido, sino una condición ambiental persistente, comparable en importancia al clima o a la carga de estrés.
Alimentación vegetal: una exposición estructural, no una intervención opcional
Durante la mayor parte de la historia humana, la dieta estuvo dominada por plantas. No como suplemento ocasional ni como elección cultural consciente, sino como base estructural de la supervivencia. Esto implicaba una exposición diaria y prolongada a una enorme diversidad de compuestos vegetales, muchos de los cuales no tenían valor energético directo ni efectos agudos evidentes.
La investigación nutricional moderna ha tendido a centrarse en aquellos componentes fácilmente cuantificables: macronutrientes, vitaminas, minerales. Sin embargo, las plantas contienen miles de metabolitos secundarios como polifenoles, terpenos, alcaloides, lignanos etc. que interactúan con sistemas fisiológicos humanos de forma sutil pero persistente (Manach et al., 2005; Williamson, 2017).
NeuroPhytome plantea que ignorar esta dimensión reguladora de la alimentación vegetal limita nuestra comprensión de procesos como el envejecimiento cerebral, la resiliencia al estrés o la vulnerabilidad a enfermedades neurodegenerativas.
Plantas como sistemas complejos de regulación adaptativa
Para avanzar en esta hipótesis es necesario abandonar una imagen simplificada de la planta como “contenedor” de principios activos. Una planta es un sistema biológico complejo y adaptativo, cuyo metabolismo se reorganiza constantemente en respuesta al entorno.
Factores como estrés hídrico, temperatura, radiación, composición del suelo, interacción con microorganismos y exposición a contaminantes modifican de forma profunda su perfil fitoquímico (Selmar & Kleinwächter, 2013). Estas modificaciones no son ruido experimental; constituyen la forma en que la planta gestiona su propia supervivencia.
Desde la perspectiva de NeuroPhytome, este punto es crucial: la planta no transmite una señal única, sino una configuración reguladora que refleja su historia ecológica reciente. El organismo humano no recibe solo nutrientes, sino información biológica codificada en forma química.
Muchos de estos compuestos actúan como moduladores de redes fisiológicas conservadas, inflamación, metabolismo energético, señalización redox, plasticidad neuronal, sin imponer estados nuevos, pero ajustando rangos de respuesta. Este tipo de modulación resulta especialmente relevante en el sistema nervioso, donde la pérdida de calibración suele preceder a la disfunción clínica manifiesta (Calabrese, 2018; Spencer, 2010).
Fenotipos dinámicos en interacción
Ni las plantas ni los humanos pueden entenderse como entidades estáticas. Ambos son fenotipos dinámicos, cuyas características funcionales dependen del entorno.
La planta expresa un perfil fitoquímico concreto en función de su ecología. El ser humano responde a ese perfil desde su propio estado fisiológico, determinado por desarrollo, edad, genética, historia metabólica y contexto ambiental.
Cuando una persona consume una planta, no interactúan dos entidades fijas, sino dos configuraciones dinámicas. Dos fenotipos que responden, cada uno a su manera, al entorno.
Este marco ayuda a explicar por qué los efectos dietéticos son tan variables entre individuos y por qué los resultados observados en estudios poblacionales no siempre se traducen de forma directa a nivel clínico individual. La llamada “nutrición personalizada” comienza precisamente en este reconocimiento (Zeevi et al., 2015).
Co-evolución humano–planta: una presión silenciosa y persistente
Hablar de co-evolución no implica simetría ni intención. Las plantas no evolucionaron para el ser humano. Sin embargo, el ser humano evolucionó expuesto de forma constante a plantas. Esta exposición formó parte del entorno selectivo bajo el cual se configuraron múltiples sistemas fisiológicos.
Durante cientos de miles de años, la disponibilidad local de plantas, su estacionalidad y su química variable determinaron qué metabolitos entraban regularmente en el organismo humano. La fisiología humana, incluida la regulación del estrés, la respuesta inflamatoria y la plasticidad neuronal, se desarrolló bajo esta presión ambiental continua.
Desde esta perspectiva, la sensibilidad del cerebro humano a determinados compuestos vegetales no es anecdótica ni cultural. Es el resultado de una historia evolutiva compartida, en la que la exposición recurrente a reguladores vegetales fue compatible, o incluso ventajosa, para la adaptación.
NeuroPhytome propone que la ruptura de este contexto, la pérdida de diversidad vegetal y la homogeneización química de la dieta moderna, puede contribuir a la fragilidad reguladora observada en muchas patologías contemporáneas.
Plantas como transductores ecológicos
Para describir este proceso con mayor precisión, NeuroPhytome introduce el concepto de plantas como transductores ecológicos.
Un transductor no refleja pasivamente; convierte información de un dominio en otro. Las plantas transforman condiciones ecológicas –clima, suelo, contaminación, estrés– en perfiles químicos específicos. Al consumirlas, los organismos humanos incorporan esa información ecológica en forma bioquímica.
En entornos ecológicamente ricos y moderadamente estresantes, esta transducción puede favorecer la adaptación y la resiliencia. En entornos degradados, transmite estrés ambiental, contaminación y desequilibrio. En ambos casos, la planta actúa como intermediaria entre el entorno y la fisiología humana.
Este marco ayuda a comprender por qué la calidad ecológica de los alimentos vegetales importa tanto como su identidad botánica y por qué la simplificación extrema de los sistemas agrícolas tiene consecuencias que van más allá del contenido nutricional.
Relevancia clínica: ejemplos concretos y reconocibles
Este enfoque se conecta directamente con problemas clínicos bien conocidos.
En el deterioro cognitivo leve, por ejemplo, no existen tratamientos farmacológicos eficaces para la prevención. Sin embargo, patrones dietéticos ricos en diversidad vegetal se asocian de forma consistente con menor riesgo de progresión a demencia (Lourida et al., 2013; Scarmeas et al., 2009). Estos efectos no se explican por un nutriente aislado, sino por procesos reguladores acumulativos que influyen en inflamación, metabolismo energético y plasticidad neuronal.
En la inflamación crónica de bajo grado, reconocida como un eje central del envejecimiento y la neurodegeneración, la intervención farmacológica suele mostrar eficacia limitada. La alimentación vegetal diversa actúa a un nivel distinto: modula redes inflamatorias y metabólicas de forma sostenida, reduciendo la probabilidad de desregulación extrema (Furman et al., 2019).
En el estrés crónico, la variabilidad interindividual es la norma. Dietas ricas en matrices vegetales complejas se asocian con una mejor regulación del eje estrés-respuesta y menor carga alostática, sugiriendo un papel modulador sobre la resiliencia neuroendocrina (McEwen & Akil, 2020).
En todos estos casos, las plantas no “tratan” la enfermedad, sino modulan el contexto fisiológico en el que la enfermedad se desarrolla o progresa.
Del individuo a la población: la importancia del largo plazo
Muchos de estos efectos solo se hacen visibles a lo largo de años o décadas, y a menudo solo a nivel poblacional. La transición global hacia dietas altamente procesadas y pobres en diversidad vegetal coincide con un aumento sostenido de enfermedades crónicas relacionadas con disfunción reguladora.
Este paralelismo no implica causalidad simple, pero sí apunta a un desacoplamiento entre fisiología humana y entorno alimentario (Myers et al., 2017). Desde una perspectiva de salud pública, comprender estos procesos permite pensar la prevención más allá de la intervención puntual. Desde la práctica clínica, ayuda a contextualizar la variabilidad interindividual y los límites de la farmacología.
Finalidad del proyecto NeuroPhytome
NeuroPhytome no ofrece recetas ni tratamientos alternativos. Su utilidad es conceptual y aplicada.
Para el profesional de la salud, ofrece un marco para interpretar procesos de largo plazo, variabilidad interindividual y resiliencia fisiológica. Para la medicina preventiva, ayuda a formular estrategias basadas en regulación y adaptación. Para el individuo, aporta comprensión sobre la alimentación como proceso continuo, no como remedio puntual.
El valor reside en repensar los problemas que ya existen, no en prometer soluciones rápidas: NeuroPhytome ofrece un marco científicamente riguroso para entender y usar las plantas como moduladores evolutivos de la regulación neurobiológica, allí donde la farmacología clásica no puede ni quiere operar.
- Cambio de paradigma
NeuroPhytome entiende las plantas no como fuentes de principios activos aislados, sino como sistemas de señalización ecológica que interactúan con redes regulatorias humanas evolutivamente conservadas. - Integración científica real
NeuroPhytome relaciona tres capas: (i) contexto vegetal (ecología/condiciones de crecimiento), (ii) perfil químico (metaboloma como salida medible), y (iii) respuesta humana (regulación neurobiológica y variabilidad individual) en un marco coherente, explicando por qué los efectos son sutiles, acumulativos y altamente interindividuales. - Valor clínico no cubierto por la medicina clásica
Actúa sobre trayectorias de regulación neurocognitiva (atención, estrés, fatiga, vulnerabilidad), no sobre síntomas agudos ni dianas únicas, complementando y no compitiendo con la farmacología de síntesis. - Innovación tecnológica difícilmente replicable
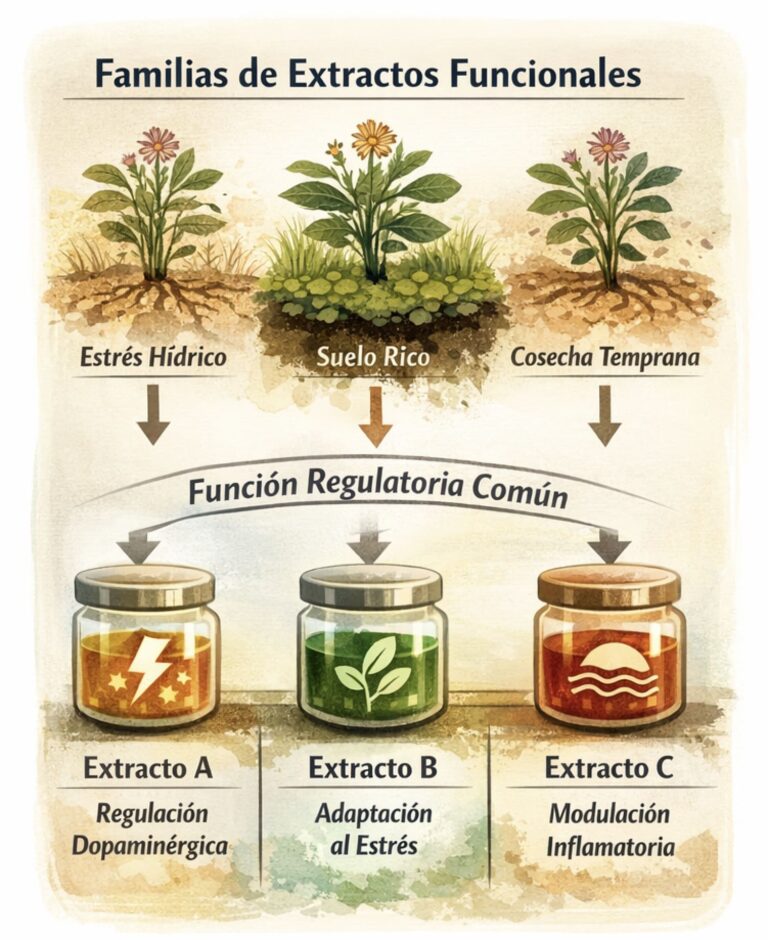
La eficacia depende de cómo vive la planta (ecología, estrés, microbiota, prácticas culturales), haciendo de la agronomía parte del resultado y permitiendo familias de extractos funcionales* y personalizables. - Impacto a largo plazo y enfoque evolutivo
Aborda la salud neurocognitiva como trayectoria adaptativa: recuperar señales regulatorias perdidas puede aumentar resiliencia y “reserva” funcional a lo largo del tiempo.
- Cambio de paradigma
En este sentido, NeuroPhytome propone una forma distinta de mirar la relación entre plantas, alimentación y cerebro. No como un conjunto de efectos aislados, sino como un proceso evolutivo, regulador y de largo plazo. Comprender este proceso no sustituye la medicina actual, pero puede ayudar a interpretarla mejor y a ampliar su horizonte preventivo.
Ese es el punto de partida de esta serie.
*Una familia de extractos funcionales se define como un conjunto de extractos derivados de una misma especie vegetal que, pese a presentar variabilidad metabolómica controlada, convergen en una función regulatoria dominante sobre sistemas biológicos humanos.
Referencias
- Calabrese, E. J. (2018). Hormesis: Path and Progression to Significance. International Journal of Molecular Sciences, 19(10), 2871. https://doi.org/10.3390/ijms19102871
- Franceschi, C., Garagnani, P., Parini, P., Giuliani, C., & Santoro, A. (2018). Inflammaging: A new immune-metabolic viewpoint for age-related diseases. Nature Reviews. Endocrinology, 14(10), 576-590. https://doi.org/10.1038/s41574-018-0059-4
- Furman, D., Campisi, J., Verdin, E., Carrera-Bastos, P., Targ, S., Franceschi, C., Ferrucci, L., Gilroy, D. W., Fasano, A., Miller, G. W., Miller, A. H., Mantovani, A., Weyand, C. M., Barzilai, N., Goronzy, J. J., Rando, T. A., Effros, R. B., Lucia, A., Kleinstreuer, N., & Slavich, G. M. (2019). Chronic inflammation in the etiology of disease across the life span. Nature Medicine, 25(12), 1822-1832. https://doi.org/10.1038/s41591-019-0675-0
- Lourida, I., Soni, M., Thompson-Coon, J., Purandare, N., Lang, I. A., Ukoumunne, O. C., & Llewellyn, D. J. (2013). Mediterranean diet, cognitive function, and dementia: A systematic review. Epidemiology (Cambridge, Mass.), 24(4), 479-489. https://doi.org/10.1097/EDE.0b013e3182944410
- Manach, C., Williamson, G., Morand, C., Scalbert, A., & Rémésy, C. (2005). Bioavailability and bioefficacy of polyphenols in humans. I. Review of 97 bioavailability studies. The American Journal of Clinical Nutrition, 81(1 Suppl), 230S-242S. https://doi.org/10.1093/ajcn/81.1.230S
- McEwen, B. S., & Akil, H. (2020). Revisiting the Stress Concept: Implications for Affective Disorders. The Journal of Neuroscience: The Official Journal of the Society for Neuroscience, 40(1), 12-21. https://doi.org/10.1523/JNEUROSCI.0733-19.2019
- Myers, S. S., Smith, M. R., Guth, S., Golden, C. D., Vaitla, B., Mueller, N. D., Dangour, A. D., & Huybers, P. (2017). Climate Change and Global Food Systems: Potential Impacts on Food Security and Undernutrition. Annual Review of Public Health, 38, 259-277. https://doi.org/10.1146/annurev-publhealth-031816-044356
- Scarmeas, N., Stern, Y., Mayeux, R., Manly, J. J., Schupf, N., & Luchsinger, J. A. (2009). Mediterranean diet and mild cognitive impairment. Archives of Neurology, 66(2), 216-225. https://doi.org/10.1001/archneurol.2008.536
- Selmar, D., & Kleinwächter, M. (2013). Influencing the product quality by deliberately applying drought stress during the cultivation of medicinal plants. Industrial Crops and Products, 42, 558-566. https://agris.fao.org/search/en/providers/122535/records/65dfceff63b8185d9caf1154?utm_source=chatgpt.com
- Spencer, J. P. E. (2010). The impact of fruit flavonoids on memory and cognition. The British Journal of Nutrition, 104 Suppl 3, S40-47. https://doi.org/10.1017/S0007114510003934
- Williamson, G. (2017). The role of polyphenols in modern nutrition. Nutrition Bulletin, 42(3), 226-235. https://doi.org/10.1111/nbu.12278
- Wyss-Coray, T. (2016). Ageing, neurodegeneration and brain rejuvenation. Nature, 539(7628), 180-186. https://doi.org/10.1038/nature20411
- Zeevi, D., Korem, T., Zmora, N., Israeli, D., Rothschild, D., Weinberger, A., Ben-Yacov, O., Lador, D., Avnit-Sagi, T., Lotan-Pompan, M., Suez, J., Mahdi, J. A., Matot, E., Malka, G., Kosower, N., Rein, M., Zilberman-Schapira, G., Dohnalová, L., Pevsner-Fischer, M., … Segal, E. (2015). Personalized Nutrition by Prediction of Glycemic Responses. Cell, 163(5), 1079-1094. https://doi.org/10.1016/j.cell.2015.11.001

Apasionado por la naturaleza, con más de 20 años de experiencia en el estudio de las plantas medicinales y su relación con la salud mental; formado en Tecnologías Alimentarias, Fitoterapia, Biología Molecular y Biomedicina.